
雌激素疗法
• 取消更年期激素替代疗法药物的“黑框”警告
• 雌激素疗法对阿尔茨海默病以及人体各器官的作用 –-综述
雄激素疗法 (待编写)
美国食品药品监督管理局取消了更年期激素替代疗法产品“黑框”警告
新闻发布室 卫生与公众服务部 11月10日 2025年
更年期激素疗法,也常被称为激素替代疗法(HRT),已被批准用于缓解常见的更年期症状,例如潮热和盗汗。由于美国食品药品监督管理局(FDA)对这些药物的风险发出“黑框”警告,导致女性可能未能充分利用这些可以缓解更年期症状并改善女性健康的已获批准的疗法。目前,F美国食品药品监督管理局正在移除这些警告。
关于激素替代疗法
激素替代疗法早已获得美国食品药品监督管理局批准,用于缓解常见的更年期症状,例如潮热和盗汗(也称为血管舒缩症状),以及由于雌激素水平下降引起的阴道、外阴和泌尿道变化所导致的症状,也称为外阴阴道萎缩或更年期泌尿生殖系统综合征。一些激素替代疗法产品也被批准用于预防骨质疏松症(骨骼变弱)。
研究表明,在更年期开始后十年内开始使用激素替代疗法可以带来诸多益处,对于大多数女性而言,这些益处大于潜在风险。益处包括降低全因死亡率和骨折风险。激素替代疗法还与心脏病发作风险降低50%、认知能力下降风险降低64%以及阿尔茨海默病风险降低35%相关。
一项对26708名女性参与者进行的30项试验的分析发现,激素替代疗法与癌症死亡率增加无关。事实上,60岁之前开始使用激素替代疗法的女性显示死亡风险有所降低。
取消“黑框”警告
美国食品药品监督管理局要求各公司修改产品标签,以提供关于这些药物益处和风险的最新、准确和平衡的信息,以便女性在咨询医疗保健提供者后,能够为自己的健康做出最佳决定。
具体而言,美国食品药品监督管理局正在与各公司合作,更新产品标签中的措辞,删除关于心血管疾病、乳腺癌和可能痴呆症风险的描述。美国食品药品监督管理局并不打算移除全身性雌激素单一制剂的子宫内膜癌黑框警告。虽然激素替代疗法 的开始时间和使用时长由处方医生和患者共同决定,但美国食品药品监督管理局 的建议是,对于全身性激素替代疗法,应在绝经后 10 年内或 60 岁之前开始使用。
此举是基于美国食品药品监督管理局对当前相关文献的评估,包括对在绝经后十年内开始接受激素替代疗法的年轻患者群体数据的重新分析。
美国食品药品监督管理局最近批准了 Premarin(结合雌激素)片剂的仿制药,Premarin 是一种复杂的雌激素混合物,用于治疗与绝经和激素缺乏相关的各种疾病。 美国食品药品监督管理局还批准了用于治疗中度至重度血管舒缩症状(例如潮热)的非激素药物。
雌激素疗法及其对不同器官系统的影响
雌激素疗法在预防绝经后女性阿尔茨海默病和痴呆症中的作用:近年综述
Noor Ali 1,2, Rohab Sohail 3, Ahmed Khawaja, et al. ✉Editors: Alexander Muacevic, John R Adler.
Cureus. 2023 Aug 6;15(8):e43053. doi: 10.7759/cureus.43053The Role of Estrogen Therapy as a Protective Factor for Alzheimer’s Disease and Dementia in Postmenopausal Women: A Comprehensive Review of the Literature
摘要
月经完全停止12个月并伴有血管舒缩症状被称为绝经。雌激素除了在生殖中发挥作用外,还显著影响中枢神经系统(CNS)。基于人群的研究表明,男性和女性的痴呆症患病率存在显著差异,其中阿尔茨海默病相关性痴呆症在女性中更为常见,这表明雌激素缺乏可能是神经退行性疾病的危险因素。痴呆症患者的神经认知功能会逐渐下降,最初表现为短期记忆丧失,随后发展为长期记忆丧失和无法进行日常活动,最终导致死亡。目前尚无治愈痴呆症的方法,因此预防或延缓疾病进展至关重要。因此,研究人员广泛研究了雌激素作为神经保护剂的作用。雌激素通过增强海马和前额叶皮层功能、减少神经炎症、防止雌激素受体降解、减少脑部氧化损伤以及增强胆碱能和血清素能功能来预防痴呆。根据窗口期假说,如果在绝经后最初五年内开始治疗,雌激素预防痴呆的效果会更加显著。然而,其他研究,例如“女性健康倡议记忆研究”(WHIMS),则显示雌激素对大脑有不利影响。本综述旨在阐明目前关于雌激素对神经退行性疾病(即痴呆和阿尔茨海默病)影响的现有数据。
引言和背景
绝经是女性体内由雌激素缺乏引起的生理现象。这种临床综合征多发于平均年龄为51岁的女性,主要表现为血管舒缩症状。由于多个身体部位均会受到影响,包括但不限于阴道、卵巢、骨骼和动脉,因此还会出现其他症状。这种生理变化始于卵巢。卵巢卵泡数量(以及卵巢储备)开始下降,导致抑制素和雌二醇水平降低。低雌二醇水平会持续对下丘脑产生正反馈。作为回应,下丘脑促性腺激素释放激素(GnRH)分泌增加,进而促进垂体分泌黄体生成素(LH)和卵泡刺激素(FSH)。这两种激素是导致更年期血管舒缩症状的主要原因。由于雌激素是子宫内膜增生的主要驱动因素,月经最初会变得不规律,最终完全停止[1]。雌激素的作用远不止于卵巢。绝经后女性除了血管舒缩症状外,还会出现许多其他症状,这便证明了这一点。雌激素有助于维持女性泌尿生殖系统的健康;因此,绝经期会出现外阴松弛、阴道口狭窄和黏膜炎症等症状。结果,女性会出现阴道干涩、阴道刺激、性交疼痛、尿失禁和尿路感染(UTI)增加等症状[2]。雌激素在骨骼生长和重塑中也发挥着重要作用。它通过激活破骨细胞和成骨细胞来刺激骨骼形成。雌激素水平降低会导致骨吸收超过骨形成[3]。这种骨骼重塑失衡会使绝经后女性面临骨量减少的风险,如果不加以控制,骨量减少会进一步发展为骨质疏松症,并增加骨折的风险[4,5]。雌激素的另一项重要功能是通过优化脂质代谢和血管阻力来预防心血管疾病。雌激素缺乏会对内膜内皮产生负面影响,导致血管收缩,并可能引发高血压。更年期还会出现低密度脂蛋白(LDL)水平加速升高,增加心血管不良事件的风险[1,4]。据估计,女性一生中超过三分之一的时间处于绝经后状态。鉴于绝经的影响广泛,且会显著影响女性的生活质量(QOL),因此,无数的研究致力于寻找预防方法和开发治疗方案,以对抗绝经后疾病并提高生活质量。然而,目前尚未取得确切的成果。目前有多种治疗方法可用于控制症状和预防疾病,包括生活方式干预(例如饮食调整)、非激素疗法(例如选择性(血清素—编者注)再摄取抑制剂)和激素疗法。美国食品药品监督管理局(FDA)已批准激素替代疗法(HRT)用于治疗血管舒缩症状,例如潮热、盗汗等。以及阴道干燥。激素替代疗法 (HRT) 可以降低绝经期女性患骨质疏松症的风险 [6-8]。尽管雌激素疗法具有积极作用,但研究表明,其疗效因年龄、种族、吸烟状况和乳腺癌病史等多种因素而存在巨大差异。医疗专业人员在开具雌激素处方之前,应全面评估每位女性接受雌激素疗法的益处和风险 [9]。
综述
雌激素疗法及其对不同器官系统的影响
雌激素疗法与心血管系统
绝经后女性的主要死因是冠心病 (CHD)。据估计,低风险女性每年每 1000 人中约有 3 至 5 例冠心病病例 [9]。1996 年,世界卫生组织 (WHO) 发布流行病学研究结果,表明与非使用者相比,使用 HRT 的女性死于冠心病的风险降低了 44%。然而,最近的一项调查——护士健康研究——显示,在考虑参与者既往心血管危险因素的情况下,使用 HRT 的女性死于冠心病的风险降低了 39%。1998 年的妇女健康倡议 (Woman’s Health Initiative) 证实了雌激素疗法的心脏保护作用。然而,与服用安慰剂的女性相比,服用持续雌激素疗法 (ET) 的女性发生静脉血栓栓塞 (VTE) 的风险更高。服用 ET 的女性中约有 5/1000 发生 VTE,而服用安慰剂的女性中约有 2/1000 发生 VTE。这种风险在前两年最高,并在七年随访期后有所下降。与此同时,1998 年的心脏和雌激素/孕激素替代研究 (HERS) 显示,在随访期间,使用者和非使用者之间的 VTE 风险没有显著差异。因此,鉴于 VTE 的持续风险,目前最好避免使用 ET 作为预防或治疗冠心病的方法。目前,控制绝经后女性冠心病的合理方法是鼓励她们保持健康的体重指数 (BMI) 并遵循有益于心脏健康的饮食 [10,11]。
(1998 年的妇女健康倡议 (Woman’s Health Initiative ) 调查用的雌激素是Premarin, 是结合型雌激素。结合型雌激素对血栓形成不良作用要比生物同源雌激素的这一作用高达2倍—编者注)
雌激素疗法与骨骼系统
绝经后,骨质减少和骨质疏松的风险增加。因此,老年女性的骨折发生率高于老年男性,其中白人女性的发生率最高,黑人女性的发生率最低。1998 年,WHIMS 研究观察到,即使在长达 13 年的随访期后,雌激素治疗 (ET) 仍能显著降低绝经后髋部骨折的风险。研究反复证实了雌激素治疗在预防绝经后骨质疏松症方面的疗效。值得注意的是,这些疗效在年龄小于 60 岁且绝经时间小于 10 年的女性中也观察到 [12-14]。
雌激素疗法与泌尿生殖系统
由于尿道黏膜和肌肉中存在雌激素受体,因此雌激素治疗可以用于治疗绝经后女性的尿失禁。此外,与口服或肠外给药途径相比,直接阴道给药(以乳膏或片剂形式)能更有效地缓解症状,因为这些剂型能将雌激素释放到阴道组织上[9]。一项纳入88名绝经后妇女的随机对照研究得出结论,阴道内雌三醇可改善尿失禁症状,并可作为激素替代疗法的替代方案。另一方面,HERS研究观察到,基线时尿失禁妇女的症状有所恶化[15,16]。
认知衰退
痴呆症是一种进行性神经退行性疾病,会影响记忆力、问题解决能力、语言能力和认知思维,最终损害日常生活能力。痴呆症的预防依赖于控制和改变危险因素的干预措施。痴呆症的致残性及其巨大的情感、心理和社会影响,使得对其进行研究成为一项至关重要且意义非凡的工作。尤其值得注意的是,痴呆症的患病率从六十岁左右的1.5%上升到九十岁左右的40%。2010年,据报道有3560万人患有痴呆症[17]。痴呆症有多种类型,例如阿尔茨海默病相关性痴呆、血管性痴呆、皮克病引起的额颞叶痴呆和路易体痴呆。阿尔茨海默病(AD)是痴呆症最常见的病因,在65岁以上人群中,其发病率每五年翻一番[18-20]。阿尔茨海默病正迅速成为美国一个重要的公共卫生问题。近期研究表明,超过400万美国人患阿尔茨海默病。据估计,每年用于照护这些患者的费用超过1000亿美元。到2050年,至少有1400万美国人将罹患此病[21]。
许多流行病学研究推测,雌激素水平下降是绝经后女性阿尔茨海默病(AD)风险增加的原因。此外,早发性绝经的女性认知能力下降速度也更快。同样,大量观察性数据支持激素替代疗法(HRT)可降低痴呆症(主要是AD)的风险。其他权威临床研究证实,在自然绝经前接受双侧或单侧卵巢切除术的患者,终生患痴呆症和认知障碍的风险更高。术后开始雌激素治疗(ET)可降低这种风险[17,22-24]。然而,妇女健康倡议(WHI)试验对这些发现提出了质疑,该试验是目前关于激素疗法认知后果的最全面的研究[22-24]。该研究表明,65岁以上服用口服雌激素(无论是否联合孕激素)的绝经后女性,患阿尔茨海默病AD的风险会增加。由于使用雌激素类激素疗法会增加心血管疾病和其他并发症的风险,该研究提前终止,且后续研究的样本量不足[23]。
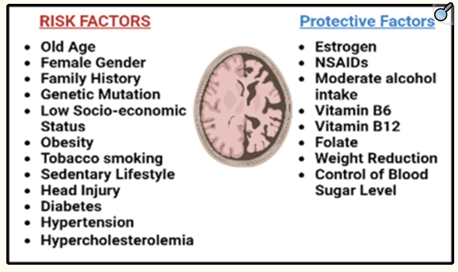
早发性阿尔茨海默病常见于携带基因突变的患者,例如唐氏综合征和载脂蛋白ε等位基因,这些基因突变使他们更容易患上这种神经系统疾病[18,19,24,25]。此外,研究发现一些可改变和不可改变的因素与疾病发展相关,例如性别(女性更常见)、家族史、生活方式(吸烟、久坐不动的生活方式)、头部损伤、低社会经济地位以及糖尿病、高血压、高胆固醇血症、肥胖、心血管疾病等[18,25-28]。一般来说,男性比女性更容易患痴呆症,但绝经后女性中阿尔茨海默病相关性痴呆的患病率更高;这促使人们发现雌激素水平低下是阿尔茨海默病的一个风险因素[9,24]。绝经后妇女的雌激素治疗、使用非甾体抗炎药治疗关节疼痛、少量饮酒、减轻体重、合理控制糖尿病和高血压,以及富含维生素B6、B12和叶酸的饮食,均与预防阿尔茨海默病的发生有关[19,21,28,29]。图1总结了与阿尔茨海默病相关的多种风险因素和保护因素。
图 1. 与阿尔茨海默病相关的诱发因素和保护因素。图片使用 BioRender.com 创建。
与阿尔茨海默病相关危险诱发因素
• 高龄 • 女性 • 家族史 • 基因突变 • 社会经济地位低下 • 肥胖 • 吸烟 • 久坐不动的生活方式 • 头部外伤 • 糖尿病 • 高血压 • 高胆固醇血症
与阿尔茨海默病相关预防保护因素
• 雌激素 • 非甾体抗炎药 • 适量饮酒 • 维生素 B6 • 维生素 B12 • 叶酸 • 减轻体重 • 控制血糖
这简单化了的因素表是根据以下原文图表:
阿尔茨海默病的首发症状是记忆障碍,主要影响短期记忆[9,18,30]。蒙特利尔认知评估量表可用于检测认知缺陷[26]。患者随后会出现词语检索困难和执行功能障碍[21]。随着疾病进展,患者会出现行为症状,例如抑郁、精神病、幻觉或错觉、空间定向障碍(在熟悉的街区迷路)、语言障碍、无法完成日常任务,最终导致患者生活不能自理,直至死亡[18,21,24,28]。研究表明,患者大脑皮层普遍萎缩,主要累及颞叶和海马体(大脑中与记忆相关的区域),并伴有脑室扩大。此外,活检显示存在神经纤维缠结和老年斑[8,18,26,30-32]。
阿尔茨海默病的病理机制始于淀粉样前体蛋白的分解,产生β-淀粉样蛋白,β-淀粉样蛋白积聚在脑血管周围,形成淀粉样斑块[8,26,32-34]。淀粉样斑块会削弱血管壁,导致颅内出血。此外,β-淀粉样蛋白对大脑也具有神经毒性作用,会破坏神经元并导致皮质萎缩[23,30,35,36]。β-淀粉样蛋白在Meynert基底核(前脑)的积聚会导致乙酰胆碱的缺失,而乙酰胆碱是记忆和学习所必需的神经递质[28,29,32]。tau蛋白(一种与微管结合的天然蛋白质,参与神经元信号传递)会从微管上脱落,并在神经元内部形成团块,抑制信号传导[23,35,37]。自由基介导的氧化损伤也参与神经退行性疾病的发生发展[28,30,34,38]。图2总结了阿尔茨海默病发生发展的所有相关机制。图 2. 阿尔茨海默病的病理机制。
随着预期寿命的提高,阿尔茨海默病的患病率显著增加[18,32]。然而,目前可用的治疗方案既不能改善也不能延缓疾病的进展[32]。由于阿尔茨海默病是唯一一种女性患病率高于男性的痴呆症,因此科学家们重点研究女性性腺激素与阿尔茨海默病之间的关系[18,21,24,37]。然而,关于雌激素在更年期相关认知衰退中的作用程度以及激素替代疗法(HRT)是否可以用于预防阿尔茨海默病仍然存在争议[39]。
雌激素
雌激素是一种类固醇激素,男女体内均可合成。在女性体内,它参与生殖系统的发育,并有助于形成第一性和第二性征。有证据表明,雌激素既具有神经保护作用,也具有神经病理作用,这使得对其进行研究变得有些复杂。有趣的是,对绝经后妇女使用激素替代疗法的研究表明,它可能对认知衰退具有保护作用,并报告称激素替代疗法可以维持脑组织完整性[25]。这些研究表明,补充雌激素可以通过促进胆碱能活性、防止毒性损伤、刺激神经元合成以及减少β-淀粉样蛋白(阿尔茨海默病中淀粉样斑块的主要成分)的沉积并增强其清除来保护认知功能[33,40]。另一方面,雌激素的促血栓形成作用可能会抵消其神经血管保护作用,因为它会增加炎症标志物和中风风险,而这两者都与痴呆症的发生发展有关[24,41]。激素替代疗法的影响被认为受多种因素影响,例如内源性雌激素暴露的时间、雌激素制剂的类型以及同时使用孕激素的情况[36]。
血清17-β雌二醇水平用于评估雌激素疗法对阿尔茨海默病和痴呆症发病机制的影响[22]。雌激素疗法中使用的雌激素作用于外周雌激素受体α,从而导致各种不良反应。一些评估非女性化雌激素的研究发现,最有效的形式含有雌激素酚环上的两个和四个碳原子。这些形式不与雌激素受体结合,但却表现出女性化雌激素的神经保护作用[42]。研究还发现,非女性化雌激素的效力是17-β雌二醇的8-114倍。因此,这些研究表明,在绝经后妇女的雌激素治疗中应使用非女性化雌激素。在接下来的章节中,我们将更深入地探讨雌激素及其受体,以及它们在阿尔茨海默病中作用的多种机制。
(非女性化或组织选择性雌激素及,例如奥培米芬 Osphena、巴泽多昔芬 Duavee和雷洛昔芬Raloxifene。–译者注)
雌激素受体
人体内存在三种类型的雌激素受体 (ER)。其中两种是细胞核受体,即受体ERα 和受体ERβ。第三种是细胞膜结合的 G 蛋白偶联受体。核受体存在于心血管系统和中枢神经系统中。它们具有转录活性,并参与与正常生理功能相关的复杂通路。ERα 特异性地存在于骨骼、乳腺、前列腺、肝脏、脂肪组织、子宫和卵巢(卵泡膜细胞)中。而 ERβ 则存在于结肠、膀胱、免疫系统、脂肪组织和卵巢(颗粒细胞)中。膜结合的 G 蛋白偶联受体缺乏转录活性,而是参与非基因组作用。它可以与其他两种核 ER 发生交叉反应。
核雌激素受体的转录活性
核受体ER 在被雌激素激活后会发生构象变化。雌激素会导致它们二聚化,从而使其能够进入细胞核并结合到特定的 DNA 序列上,从而调节雌激素反应基因的表达。核受体 ER 的功能因其在体内的表达部位而异。例如,它们参与维持细胞结构、细胞增殖和血压调节。
剪接变体
受体ER 具有多种变体,因此参与不同的器官功能,影响生理和病理过程。随着年龄的增长,剪接的 ERα mRNA 和芳香化酶的基因表达会下降,尤其是在与记忆和学习相关的脑区。这种变化也见于阿尔茨海默病患者,这表明雌激素在阿尔茨海默病的病理生理学中发挥着作用 [34]。
线粒体功能障碍
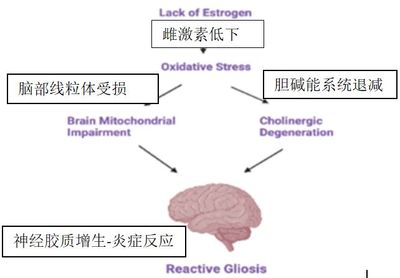
脑线粒体参与脑能量产生、氧化应激调节和细胞凋亡。氧化应激随着年龄增长而加剧,导致活性氧(ROS)积累,进而损伤脂质、蛋白质和线粒体DNA。氧化应激引起的线粒体功能障碍是衰老大脑和许多神经退行性疾病(包括阿尔茨海默病)中观察到的首个病理变化。蛋白质组学研究强调了雌激素在线粒体表达中的作用。绝经后妇女长期缺乏雌激素不仅会导致雌激素受体表达改变,还会加剧大脑氧化应激,从而导致线粒体功能障碍和胆碱能神经元退化,最终导致反应性胶质增生,如图3所示。因此,脑线粒体被认为是雌激素神经保护作用的靶点[43]。
图 3. 更年期期间的线粒体功能障碍
雌激素与胆碱能系统
神经内分泌学研究表明,胆碱能系统在记忆和学习中发挥着重要作用。特别是隔核-海马胆碱能通路。阿尔茨海默病 (AD) 患者的胆碱能系统(即乙酰胆碱和胆碱乙酰转移酶活性)会下降,而绝经后妇女的长期雌激素治疗 (ET) 试验表明,其胆碱能功能有所改善。此外,类似试验还观察到对多巴胺能和血清素能神经递质的反应性增强。诚然,这些研究存在局限性;它们没有直接分析雌激素对下丘脑-垂体轴受体反应的影响。此外,这些研究是观察性研究和横断面研究 [44]。正电子发射断层扫描 (PET) 和功能性磁共振成像 (fMRI) 等神经影像学证据表明,雌激素可以通过改变海马体和前额叶皮层来增强记忆 [45]。巴尔的摩老年人纵向研究也观察到了同样的结果。其后续研究考察了激素疗法三年来的影响,结果显示,与未接受激素替代疗法 (HRT) 的女性相比,接受 HRT 的女性大脑多个区域的血流量增加,包括海马体、右侧海马后皮层和右侧内嗅皮层 [45]。鉴于上述情况,一些研究建议将胆碱能增强药物与雌激素治疗联合使用,以治疗患有轻度认知障碍早期症状的绝经后老年女性。
阿尔茨海默病中的神经炎症
神经炎症是阿尔茨海默病发病机制中的主要机制。据报道,雌激素可以通过降低促炎细胞因子的水平来减轻炎症。雌激素还能刺激小胶质细胞产生抗炎细胞因子。一项试验报告称,雌激素治疗自身免疫性脑脊髓炎雌性小鼠可降低促炎细胞因子 TNFα、IFN-γ 和趋化因子的表达。基线雌激素水平较低的卵巢切除雌性小鼠这些细胞因子的表达增加。因此,雌激素缺乏会导致细胞因子和炎症标志物增加。此外,ERβ受体激动剂似乎会影响白细胞介素(如 IL-6、IL-1β 和 IL23-p19)的水平,并产生一氧化氮合酶 (NOS),从而减少星形胶质细胞和小胶质细胞介导的炎症反应。而 ERα 受体激动剂可下调小鼠的趋化因子、小胶质细胞活化、星形胶质细胞增生和 T 细胞浸润,因此雌激素具有神经保护作用 [34]。图 4 描述了雌激素缺乏的细胞反应。
图 4. 雌激素缺乏的细胞效应。
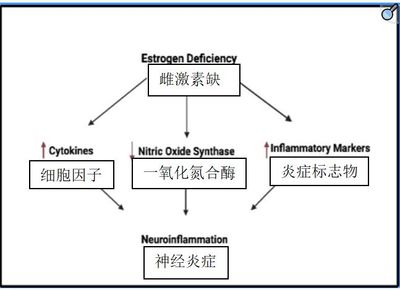
卵巢切除的小鼠接受β-淀粉样蛋白 注射后,表现出小胶质细胞增生、星形胶质细胞增生和核因子 kappa-B (NF-κB) 激活的增加。此外,在人脑中,雌激素给药增加了小胶质细胞对β-淀粉样蛋白 i的清除,强调了雌激素在小胶质细胞介导的β-淀粉样蛋白 清除中发挥的作用,从而导致炎症的下调 [34]。(β-淀粉样蛋白是导致阿尔茨海默病的一个重要病理机制—译者注)
阿尔茨海默病与 APOE4 基因的多态性
APOE 基因型与阿尔茨海默病AD 和认知能力下降的风险密切相关。与野生型 APOE3/E3 相比,APOE3/E4 和 APOE4/E4 基因型的人患阿尔茨海默病AD 的风险分别增加 3-4 倍和 12-15 倍 [46]。超过一半的 AD 患者表达 APOE4。有趣的是,APOE2 已被证明具有神经保护作用。在人类中,APOE4 有三种亚型:APOE2、APOE3 和 APOE4,其流行率分别约为 10%、80% 和 14%。Apo E 存在于大脑中,并在脑脊液中充当脂质转运蛋白。雌激素参与胆固醇和脂质转运,并调节低密度脂蛋白受体相关蛋白,该蛋白在β-淀粉样蛋白( Aβ) 的产生和清除中发挥作用。脂蛋白受体相关蛋白 1与 APOE4 之间的结合较弱,会损害 Aβ 的清除,并导致 AD 中的神经炎症。许多研究表明,携带 APOE4 基因的女性与激素替代疗法 (HRT) 相关的阿尔茨海默病(AD) 发展之间存在上述关系。在携带 APOE4 突变的绝经后女性中使用 HRT 可以减少β-淀粉样蛋白沉积 [34]。Saleh 等人进行了一项研究,揭示了 APOE 基因型和开始 HRT 的年龄对认知功能、与认知相关的脑容量及其不同结果的影响。研究结果表明,APOE4 女性对 HRT 的反应最显著。与未使用 HRT 的 APOE4 女性相比,她们的内嗅皮层和杏仁核体积更大,并且可重复神经心理状态评估量表 (RBANS) 延迟记忆指数得分更高。此外,APOE4基因型女性开始激素替代疗法(HRT)的年龄越早,海马体体积越大。早期研究表明,APOE4基因型女性的脑血流量(CBF)更高。因此,HRT的反应可以被描述为APOE基因依赖性的[46]。
机会窗口理论
多项研究表明,存在一个最佳时期,或者说是一个“机会窗口”,在此期间进行激素治疗可以改善绝经后女性的认知功能[25,36,41,47,48]。这个时期被认为是围绝经期或绝经后不久,特别是绝经后的前五年[48]。基于各种观察性和干预性临床研究,有几个原因可以解释这一点。首先,较长的绝经前阶段与更好的认知功能和较低的阿尔茨海默病(AD)风险相关。绝经前每增加一个月的使用雌激素,阿尔茨海默病的风险就会降低0.5%[49]。其次,随着低雌激素阶段的延长,雌激素受体(ER)的数量和亲和力会降低,尤其是ERα[31,49,50]。阿尔茨海默病患者的ERα数量与认知功能之间存在直线关系,这进一步支持了“ERα降解”的观点,以及在一定时期后开始激素治疗会导致疗效不佳、无效甚至产生负面结果[49]。在妇女健康倡议记忆研究(WHIMS)中就观察到了这种不利结果,该研究发现,65岁及以上服用连续联合激素治疗的绝经后女性认知障碍的风险显著增加;WHIMS-MRI研究也显示,服用激素治疗的老年女性比未服用激素治疗的女性脑萎缩更严重[50,51]。同样,Whitmer等人进行的一项研究表明,在48.7岁开始HRT可以降低26%的痴呆风险,而在76岁开始HRT则会增加48%的风险[52]。此外,2016年一项使用最佳判别体素分析(ODVBA)评估激素治疗相关脑结构变化的研究发现,接受激素治疗的女性灰质发生了不利变化[53]。有研究推测,雌激素疗法的这些不良反应可能是因为先前的较低的基础认知水平,或先前已经存在的神经系统退行性病变有关[51]。
值得一提的是,大多数将雌激素疗法与降低阿尔茨海默病风险联系起来的研究都是针对年轻女性进行的。鉴于内源性雌激素具有积极的神经认知保护作用,与绝经后期相比,绝经初期神经损伤较少,因此更有可能延缓或预防轻度认知障碍,并最终预防阿尔茨海默病[23,36]。例如,2016年的一项随机激素疗法试验比较了近期绝经女性接受经皮17β-雌二醇治疗的情况。
结论
平均而言,女性的寿命比男性长,而且她们生命中有相当一部分时间处于绝经后状态。因此,雌激素缺乏导致的诸多负面变化威胁着女性的生活质量。认知能力下降是其中一个主要问题,这对初级保健和女性健康服务提供者构成了时间紧迫的挑战。尽管实验室研究表明雌激素疗法对认知功能具有积极作用,但这一结论尚未在人体研究中得到强有力且明确的证实。迄今为止,单独使用雌激素疗法(即不联合使用孕激素),仅用于预防阿尔茨海默病和痴呆症,似乎最有利于65岁以下、认知功能正常的健康围绝经期女性。鉴于目前关于激素替代疗法(HRT)最佳疗程的研究较少,且已知雌激素具有促血栓形成作用,因此治疗时长应由医生根据对患者的初始和后续评估来决定。根据已有的文献,雌激素主要起保护作用,而非治疗作用。为了证实这一点,并将雌激素疗法纳入女性痴呆症的预防管理,我们需要开展更大规模的研究,专门针对具有认知能力下降风险因素的女性,例如有痴呆症家族史或早发性痴呆症的女性、APOE4基因携带者、早发性绝经女性(例如卵巢早衰患者)以及患有脑血管疾病的女性。此外,我们注意到雌激素参与神经保护信号通路。所有信号通路都需要酶和/或辅因子,而这些又需要维生素。因此,在研究雌激素对认知功能的影响之前,纠正维生素缺乏至关重要。
引用的文献在本译文省略。请原谅。需追踪文献可根据提供的原文链接查取。